想注册申报特医食品,看看需要提交那些资料?
作者:冬泽特医
发布时间:2021-05-12 13:07:47
浏览次数:3346
按照《食品安全法》的规定,特殊医学用途配方食品(特医食品)需要向国家市场监督管理总局(SMAR)申请注册,拿到注册证书后才被允许在中国市场生产销售。
特医食品是为了满足特殊人群对营养素或膳食的特殊需求,而专门加工配制的配方食品,通常为粉状或液态的食品。

特医食品研发流程及注册申报
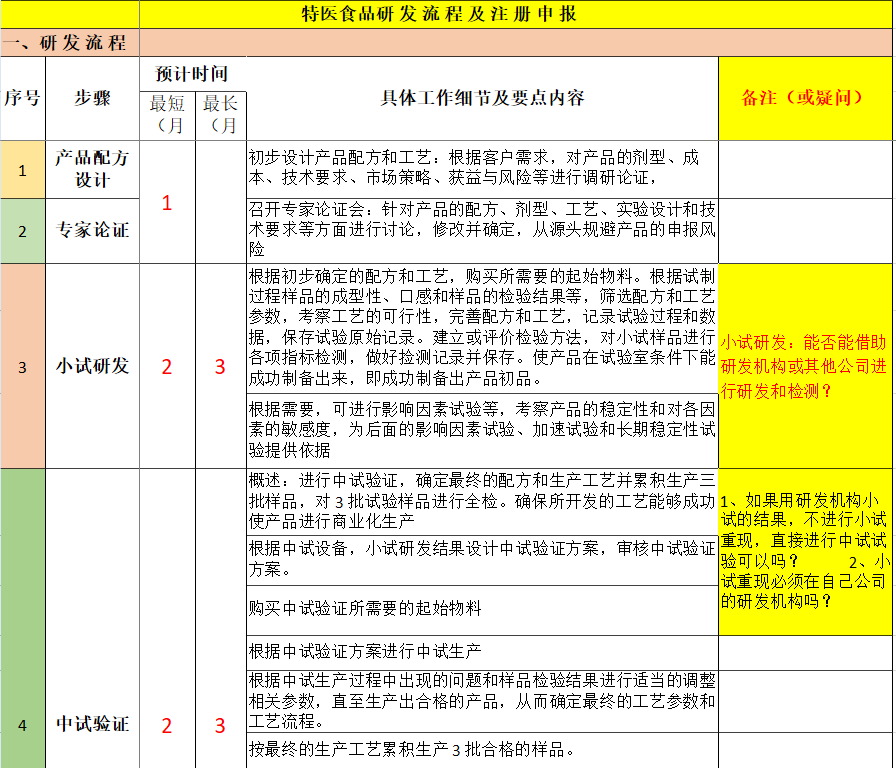
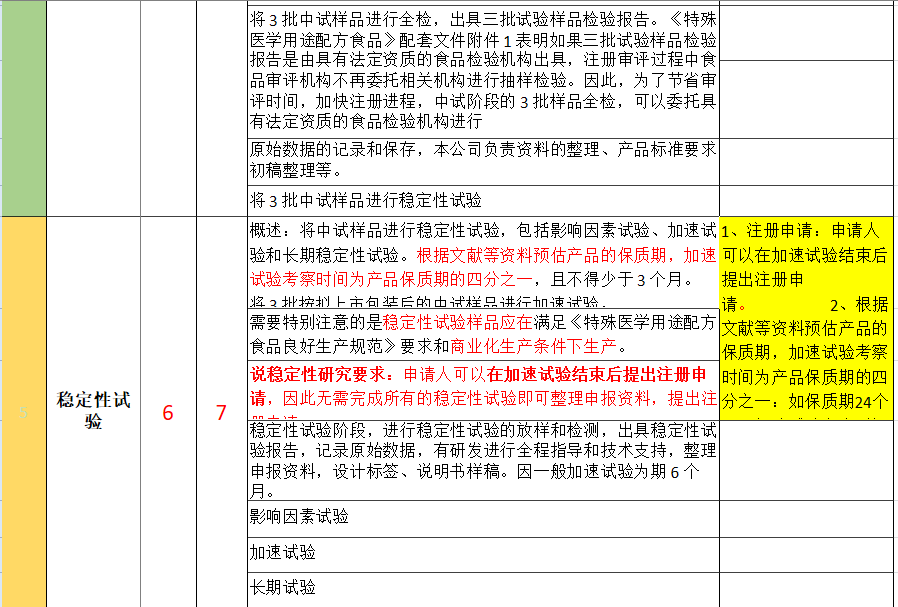
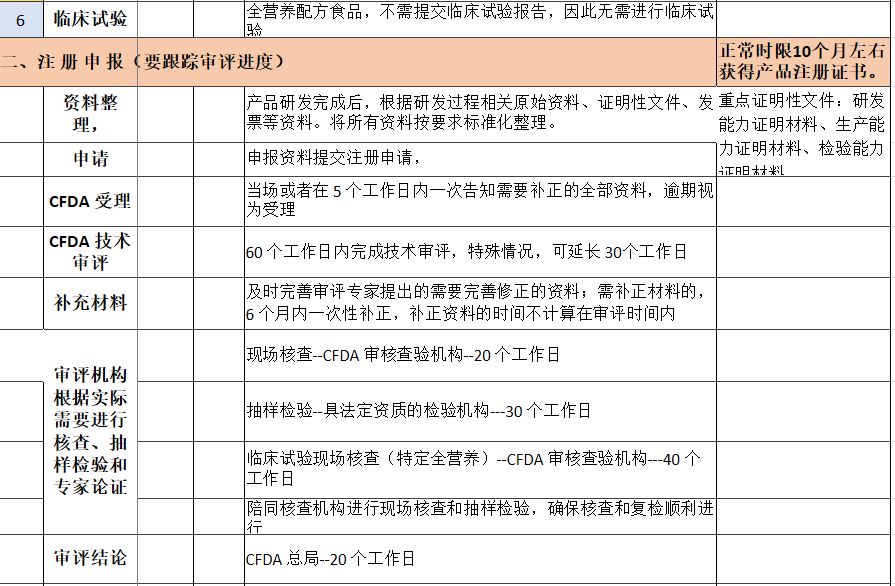

申请特殊医学用途配方食品注册需要提交哪些资料?
- 特殊医学用途配方食品注册申请书
- 产品研发报告和产品配方设计及其依据
- 生产工艺资料
- 产品标准要求
- 产品标签、说明书样稿
- 试验样品检验报告
- 研发、生产和检验能力证明材料
- 其他表明产品安全性、营养充足性以及特殊医学用途临床效果的材料
-
申请特定全营养配方食品注册,还应当提交临床试验报告
- 产品生产国(地区)政府主管部门或者法律服务机构出具的境外申请人为境外生产企业的资质证明文件复印件及其中文译本。
- 产品生产国(地区)政府主管部门或者法律服务机构出具的允许产品上市销售的证明复印件及其中文译本,产品未上市销售的,可不提供。
- 由境外申请人常驻中国代表机构办理注册事务的,应当提交《外国企业常驻中国代表机构登记证》复印件。
- 境外申请人委托境内代理机构办理注册事项的,应当提交经过公证的授权委托书原件及其中文译本,以及受委托的代理机构营业执照复印件。
特殊医学用途配方食品注册申报需要提交哪些检测报告?
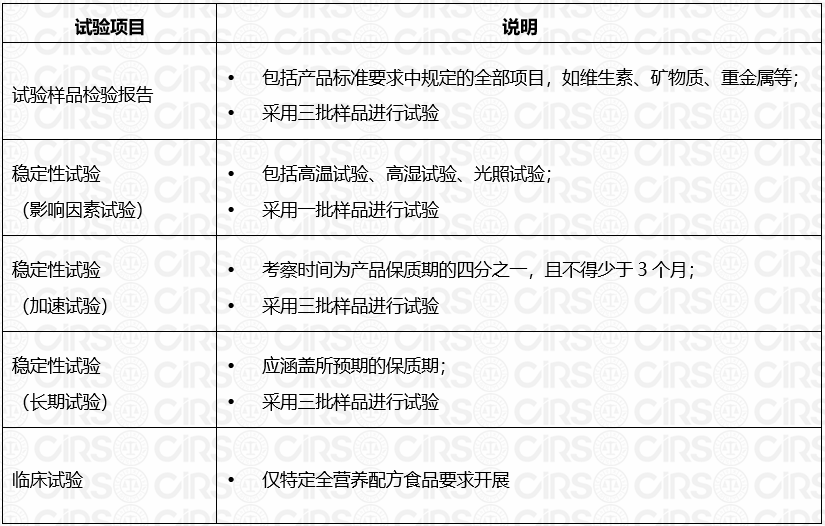
注意:不同的特医食品类别在首次申请注册的时候,需要提交的检测报告要求不同。
特殊医学用途配方食品注册申报流程
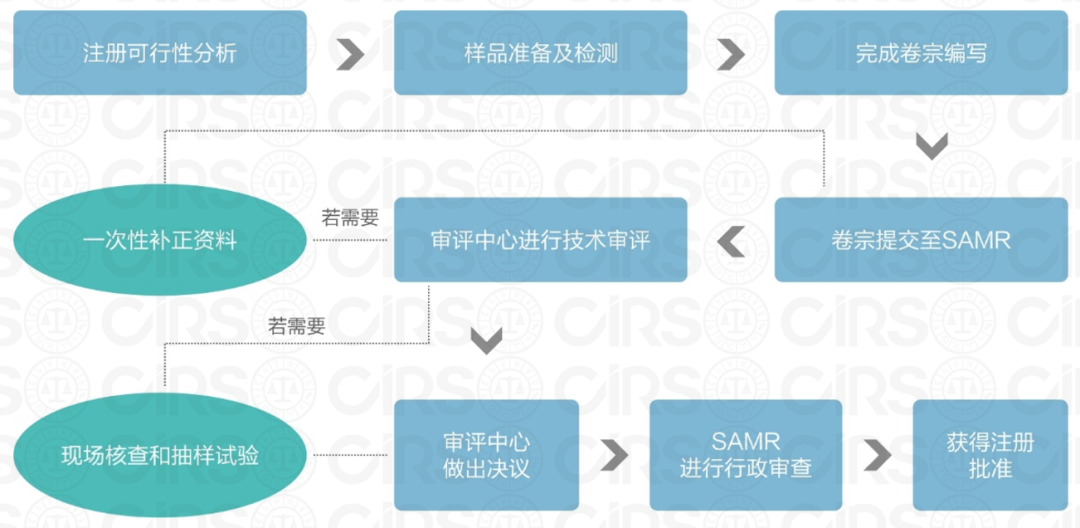
特殊医学用途配方食品注册申报周期
从初期的资料准备到检测到官方审评,全营养配方食品、非全营养配方食品、特殊医学用途婴儿配方食品的注册申报周期通常为1到2年。特定全营养配方食品因为需要安排临床试验,因此整个申报周期至少在3年以上(拜仑斯特)。
文章来自网络,如侵删
- 胃肠特医国标立项!特定全营... 2026-04-15
- 导语:在特殊医学用途配方食品行业飞速发展的当下,市场始终陷入一种看似繁荣的结构性矛盾:一边是全营养配方扎堆上市、渠道竞争白热化,产品...【详细】

